PHARMA MAR
- Cobreti
- Mensajes: 27
- Registrado: 25 Feb 2019 23:43
- Agradecido: 30 veces
- Agradecimiento recibido: 17 veces
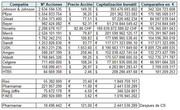
Os dejo una tablita que me he ido haciendo, para tener una visión.
https://ibb.co/CWKTpcT
(perdón, que aun no domino el subir imágenes a los post...)
Se aceptan nuevas empresas a añadir para ampliar la tabla.
Voy a ir ampliando información considerando el % de volumen de negocio para cada empresa por sector, de modo que se pueda comparar la parte relativa a negocio similar.
Pero como primer tiro, espero que pueda serviros :)
Como datos, para la comparativa se ha usado el cambio:
€-CHF 0.93
€-$ 0.87
€-£ 1.1
https://ibb.co/CWKTpcT
(perdón, que aun no domino el subir imágenes a los post...)
Se aceptan nuevas empresas a añadir para ampliar la tabla.
Voy a ir ampliando información considerando el % de volumen de negocio para cada empresa por sector, de modo que se pueda comparar la parte relativa a negocio similar.
Pero como primer tiro, espero que pueda serviros :)
Como datos, para la comparativa se ha usado el cambio:
€-CHF 0.93
€-$ 0.87
€-£ 1.1
- Himbersor
- Mensajes: 423
- Registrado: 25 Feb 2019 14:17
- Agradecido: 50 veces
- Agradecimiento recibido: 433 veces
No la has subido bien. Tienes que copiar todo el enlace que te sale abajo en la página de subir imágenes. Si la quieres meter aquà le das al cuadrito de insertar imagen y pones la dirección ahi
- kuky24
- Mensajes: 501
- Registrado: 25 Feb 2019 15:32
- Agradecido: 58 veces
- Agradecimiento recibido: 41 veces
PharmaMar sube en bolsa tras solicitar a Suiza comercializar la lurbinectedina
Empresas- 20/07/2020 16:39:01
PharmaMar ha anunciado que ha presentado a la Agencia Suiza de Productos Terapéuticos la "Autorización Temporal" para la comercialización de lurbinectedina para el tratamiento de pacientes con cáncer de pulmón microcÃtico que han progresado después de una terapia previa basada en platino. Un hecho que la está impulsando en bolsa, a estas horas del lunes sus tÃtulos suben cerca de un 3%
Empresas- 20/07/2020 16:39:01
PharmaMar ha anunciado que ha presentado a la Agencia Suiza de Productos Terapéuticos la "Autorización Temporal" para la comercialización de lurbinectedina para el tratamiento de pacientes con cáncer de pulmón microcÃtico que han progresado después de una terapia previa basada en platino. Un hecho que la está impulsando en bolsa, a estas horas del lunes sus tÃtulos suben cerca de un 3%
- kuky24
- Mensajes: 501
- Registrado: 25 Feb 2019 15:32
- Agradecido: 58 veces
- Agradecimiento recibido: 41 veces
Esta solicitud de registro se basa en los datos del ensayo basket de fase II con lurbinectedina, en monoterapia, para el tratamiento de cáncer de pulmón microcÃtico. Los datos, que fueron publicados en la edición de mayo de 2020 de The Lancet Oncology[1], mostraron que en cáncer de pulmón microcÃtico recurrente lurbinectedina demostró una Tasa de Respuesta Global (ORR, Overall Response Rate) del 35% y una mediana de la Duración de la Respuesta de 5,3 meses, según la evaluación del investigador (30% y 5,1 meses respectivamente, según la medición del Comité de Revisión Independiente.
En determinadas condiciones, Suiza concede una autorización temporal para poner a disposición de los pacientes lo antes posible medicamentos para el tratamiento de enfermedades que ponen en peligro su vida. Se trata de un procedimiento simplificado con plazos generales más cortos que los de un procedimiento de registro estándar. No debe haber ningún medicamento alternativo autorizado o disponible en Suiza. Se espera un beneficio terapéutico importante del uso del producto para el que se solicita la autorización.
En determinadas condiciones, Suiza concede una autorización temporal para poner a disposición de los pacientes lo antes posible medicamentos para el tratamiento de enfermedades que ponen en peligro su vida. Se trata de un procedimiento simplificado con plazos generales más cortos que los de un procedimiento de registro estándar. No debe haber ningún medicamento alternativo autorizado o disponible en Suiza. Se espera un beneficio terapéutico importante del uso del producto para el que se solicita la autorización.
- Estos usuarios agradecierón al autor kuky24 por el mensaje (total 3):
- Salomón_7 • tuca • Trinraf
- kuky24
- Mensajes: 501
- Registrado: 25 Feb 2019 15:32
- Agradecido: 58 veces
- Agradecimiento recibido: 41 veces
27/07/2020
12:54:58 PharmaMar firma un acuerdo con Adium para comercializar Yondelis en Latinoamérica
PharmaMar ha anunciado este lunes un acuerdo de licencia con Adium Pharma para comercializar el fármaco antitumoral de origen marino Yondelis en Argentina, Bolivia, Brasil, Chile, Colombia, Costa Rica, Curazao, República Dominicana, Ecuador, El Salvador, Guatemala, Honduras, Jamaica, México, Nicaragua, Panamá, Paraguay, Perú, Trinidad y Tobago, Uruguay y Venezuela. La compañÃa está cayendo hoy con fuerza en bolsa (-8,4%).
12:54:58 PharmaMar firma un acuerdo con Adium para comercializar Yondelis en Latinoamérica
PharmaMar ha anunciado este lunes un acuerdo de licencia con Adium Pharma para comercializar el fármaco antitumoral de origen marino Yondelis en Argentina, Bolivia, Brasil, Chile, Colombia, Costa Rica, Curazao, República Dominicana, Ecuador, El Salvador, Guatemala, Honduras, Jamaica, México, Nicaragua, Panamá, Paraguay, Perú, Trinidad y Tobago, Uruguay y Venezuela. La compañÃa está cayendo hoy con fuerza en bolsa (-8,4%).
- Sieben
- Mensajes: 44
- Registrado: 25 Feb 2019 08:18
- Agradecido: 86 veces
- Agradecimiento recibido: 59 veces
Alguien ha leÃdo novedades sobre la Nurbenectedina?
https://www.diariomedico.com/medicina/e ... mamar.html
Según este artÃculo acabarÃa de ser aprobado por la FDA
https://www.diariomedico.com/medicina/e ... mamar.html
Según este artÃculo acabarÃa de ser aprobado por la FDA
- jmaliste
- Mensajes: 67
- Registrado: 24 Feb 2019 23:22
- Agradecido: 2 veces
- Agradecimiento recibido: 12 veces
esto es lo que pone en el articulo por si no lo podeis leer.
Empresas - Luis Mora, director general de la Unidad de Negocio de OncologÃa
Lurbenectedina puede ser el punto de inflexión para PharmaMar
El compuesto acaba de recibir la aprobación de la FDA para el cáncer de pulmón microcÃtico en segunda lÃnea.
Luis Mora, director general de la Unidad de Negocio de OncologÃa de PharmaMar, explica que lurbinectedina está revelando actividad también en varios otros tipos de cáncer.
Luis Mora, director general de la Unidad de Negocio de OncologÃa de PharmaMar, explica que lurbinectedina está revelando actividad también en varios otros tipos de cáncer.
Cristina G. Real
Lun, 27/07/2020 - 07:00
La biotecnológica española PharmaMar lleva más de tres décadas explorando las posibilidades terapéuticas de los organismos que extrae del fondo marino. Tras varios años de investigación, debutó en el mercado en 2007 con el afamado Yondelis –trabectedina– para sarcoma de tejidos blandos. El camino hasta su aprobación fue largo y tortuoso; no en vano se trataba de demostrar por primera vez la actividad terapéutica de un antineoplásico sintético aislado originalmente del tunicado marino Ecteinascidia turbinata, y de aportar la información necesaria para que las agencias reguladoras pudieran evaluar un compuesto cuyo origen nunca antes habÃan valorado.
Sin embargo, el producto transformador para PharmaMar puede ser el que ahora llega al mercado estadounidense tras su aprobación por la FDA hace unas semanas. Zepzelca -lurbinectedina-, también aislado de la Ecteinascidia turbinata, ha recibido el visto bueno de la agencia norteamericana para el tratamiento en segunda lÃnea del cáncer de pulmón microcÃtico o de células pequeñas, y la compañÃa ha solicitado ya la aprobación para esta indicación también a la agencia reguladora suiza. Luis Mora, director general de la Unidad de Negocio de OncologÃa de PharmaMar, explica que este compuesto no solo llega al mercado con una indicación mucho menos nicho que la primera de Yondelis, sino que, además, "es una indicación para la que no hay tantas alternativas terapéuticas". Por si no fueran suficientes avales, "lurbinectedina está revelando actividad en varios otros tipos de cáncer", añade.
La 'Ecteinascidia turbinata' es el tunicado marino a partir del que se ha aislado lurbinectedina.
La 'Ecteinascidia turbinata' es el tunicado marino a partir del que se ha aislado lurbinectedina.
La vÃa de administración es otra de las ventajas de lurbinectedina frente a otras alternativas para el cáncer de pulmón microcÃtico, ya que el paciente recibe el tratamiento en una hora de infusión cada tres semanas, es decir, "de manera mucho más eficiente en términos de calidad de vida".
El medicamento se ha registrado para Estados Unidos a través de un acuerdo de licencia alcanzado entre PharmaMar y Jazz Pharmaceuticals que está valorado en más de mil millones de dólares, de los cuales la biotecnológica española ha cobrado ya unos 300 millones por la firma del acuerdo y la aprobación de la FDA, y aún recibirá "cobros adicionales derivados de otros hitos que se van a producir en el futuro, además de importantes royalties por la venta del producto en Estados Unidos".
Mora recuerda que el norteamericano representa más del 55% del mercado mundial de productos de oncologÃa. A raÃz de esta aprobación, PharmaMar está hablando con potenciales socios en otras partes del mundo, donde ya tiene acuerdos para el sudeste asiático, Australia y China. "En Europa, el proceso regulatorio es diferente, aunque estamos en contacto con las autoridades para ver cuál es la mejor vÃa de registro aquÃ. No obstante, hemos abierto programas de uso compasivo o de medicación extranjera, para que también los pacientes en Europa puedan tener ya acceso al medicamento. En el primer semestre de este año -añade Mora-, ya hemos tratado a más de 600 pacientes en España, Francia y Holanda gracias al programa abierto de uso compasivo", lo que supone en su opinión "un dato increÃble que da idea de la gran necesidad que hay y de que es un producto que están aceptando muy bien los oncólogos".
La FDA designa medicamento huérfano a lurbinectedina para cáncer de pulmón microcÃtico
"Aplidin es el antiviral más potente que se ha descrito jamás"
'Yondelis' (PharmaMar) llegará por primera vez a Australia y Nueva Zelanda
De momento, la aprobación de la FDA convierte a Zepzelca en "el primer fármaco en llegar al mercado desde hace 24 años para la segunda lÃnea" de tratamiento del citado cáncer. "Esto nos pone en una posición de ventaja frente a competidores futuros, aunque no se prevén para los próximos tres años al menos en esta segunda lÃnea de tratamiento, por lo que, desde el punto de vista comercial, hay un espacio muy grande para el crecimiento del producto. Además, en oncologÃa llegar el primero es importante porque ya eres referente y te conviertes en tratamiento estándar, es decir, los productos posteriores que opten a la aprobación para la misma indicación tendrán que compararse con el primero, y superarlo tanto en actividad como en seguridad".
En cierto modo, PharmaMar ya ha experimentado esto con Yondelis para sarcoma en Europa, indicación con la que sigue manteniendo la misma cuota de mercado -del 30 al 35% en segunda lÃnea- desde su aprobación. "Después, otros productos se han aprobado para ese sarcoma, pero Yondelis mantiene la cuota inicial, es decir, se ha posicionado ya como un tratamiento de referencia para esa patologÃa".
El directivo recuerda cómo Yondelis marcó un hito en su dÃa porque fue la prueba de concepto de que el mar es una fuente de fármacos, y de que PharmaMar es capaz de desarrollarlos. Ahora, lurbinectedina marca su propio hito a otro nivel. "En Europa hay aproximadamente 12.000 diagnósticos anuales de sarcoma -para el está indicadoYondelis-, frente a los 65.000 de cáncer de pulmón microcÃtico que se diagnostican anualmente".
Comportamiento en el mercado
PharmaMar estima que pasados los primeros seis meses desde su introducción en el mercado americano podrá disponer de información suficiente para valorar la aceptación del compuesto y su comportamiento en el mercado ya en condiciones de uso real. "De aquà a final de año tendremos datos, aunque hay que ver cómo se comporta el mercado en la circunstancia actual provocada por la pandemia de Covid-19. En condiciones normales, entre 6 y 9 meses son suficientes para observar una tendencia fidedigna, aunque en Estados Unidos el posicionamiento definitivo se alcanza al tercer año", comenta Mora.
Pero el potencial de lurbinectedina se verá también con esas otras indicaciones para las que se está desarrollando, "en las que hay una necesidad médica importante –como mesotelioma y cáncer de endometrio- y para las que ha demostrado en estadios primarios de desarrollo una actividad interesante". PharmaMar está desarrollando esas otras indicaciones también con su socio Jazz, y ambas están trabajando en combinaciones de lurbinectedina con algunos productos de inmunoterapia, "demostrando con los primeros datos que están llegando una sinergia muy importante".
Su llegada al mercado constituye, por otra parte, "un espaldarazo muy importante para potenciar la investigación de la compañÃa, ya que en lo que queda de este año y en 2021 nuevos productos procedentes de nuestra investigación interna empezarán las fases clÃnicas", comenta el portavoz de PharmaMar, que también está trabajando para incorporar un nuevo producto de investigación externa a su red de ventas en Europa. Sin este espaldarazo esos nuevos productos entrarÃan en la clÃnica de uno en uno, mientras que la situación actual hace que este año sean tres los que van a empezar este proceso". En la actualidad, la biotecnológica tiene una cartera con más de 1.500 patentes fruto de su investigación, y filiales comerciales en varios paÃses de Europa.
Impacto económico
En definitiva, toda esta estrategia ha permitido a la compañÃa pagar dividendos recientemente -algo que Mora no recuerda que haya pasado con anterioridad después de 20 años en PharmaMar-, "y nuestro objetivo es tener una continuidad como negocio sostenible a futuro con incrementos de Ebitda que permitan esta nueva era", comenta e insiste, por último, en la definición de lurbinectedina como "un producto que nos transforma de ser una compañÃa con un solo compuesto en el mercado que comercializa directamente, a ser una compañÃa con indicaciones más grandes y con tres productos en el mercado en los próximos dos años, y que además se alimentará de importantes pagos de los socios por royalties, hitos, etc. Es decir, en dos años PharmaMar será otra empresa, fruto en gran medida de su apuesta por la investigación -más de 70 millones al año para poder llevar a cabo ensayos clÃnicos- hace algunos años cuando estaba en pérdidas".
En este sentido, Mora concluye que "se ha demostrado que los paÃses que han apostado por la investigación tienen una posición mucho más resistente y economÃas más saludables que la nuestra; originan patentes, acuerdos, traen dinero de fuera al paÃs y generan externalidades muy positivas y empleo de calidad", y pone el ejemplo de PharmaMar cuya plantilla está formada en un 85% por titulados universitarios, de los cuales el 22% son doctores en distintas materias.
Empresas - Luis Mora, director general de la Unidad de Negocio de OncologÃa
Lurbenectedina puede ser el punto de inflexión para PharmaMar
El compuesto acaba de recibir la aprobación de la FDA para el cáncer de pulmón microcÃtico en segunda lÃnea.
Luis Mora, director general de la Unidad de Negocio de OncologÃa de PharmaMar, explica que lurbinectedina está revelando actividad también en varios otros tipos de cáncer.
Luis Mora, director general de la Unidad de Negocio de OncologÃa de PharmaMar, explica que lurbinectedina está revelando actividad también en varios otros tipos de cáncer.
Cristina G. Real
Lun, 27/07/2020 - 07:00
La biotecnológica española PharmaMar lleva más de tres décadas explorando las posibilidades terapéuticas de los organismos que extrae del fondo marino. Tras varios años de investigación, debutó en el mercado en 2007 con el afamado Yondelis –trabectedina– para sarcoma de tejidos blandos. El camino hasta su aprobación fue largo y tortuoso; no en vano se trataba de demostrar por primera vez la actividad terapéutica de un antineoplásico sintético aislado originalmente del tunicado marino Ecteinascidia turbinata, y de aportar la información necesaria para que las agencias reguladoras pudieran evaluar un compuesto cuyo origen nunca antes habÃan valorado.
Sin embargo, el producto transformador para PharmaMar puede ser el que ahora llega al mercado estadounidense tras su aprobación por la FDA hace unas semanas. Zepzelca -lurbinectedina-, también aislado de la Ecteinascidia turbinata, ha recibido el visto bueno de la agencia norteamericana para el tratamiento en segunda lÃnea del cáncer de pulmón microcÃtico o de células pequeñas, y la compañÃa ha solicitado ya la aprobación para esta indicación también a la agencia reguladora suiza. Luis Mora, director general de la Unidad de Negocio de OncologÃa de PharmaMar, explica que este compuesto no solo llega al mercado con una indicación mucho menos nicho que la primera de Yondelis, sino que, además, "es una indicación para la que no hay tantas alternativas terapéuticas". Por si no fueran suficientes avales, "lurbinectedina está revelando actividad en varios otros tipos de cáncer", añade.
La 'Ecteinascidia turbinata' es el tunicado marino a partir del que se ha aislado lurbinectedina.
La 'Ecteinascidia turbinata' es el tunicado marino a partir del que se ha aislado lurbinectedina.
La vÃa de administración es otra de las ventajas de lurbinectedina frente a otras alternativas para el cáncer de pulmón microcÃtico, ya que el paciente recibe el tratamiento en una hora de infusión cada tres semanas, es decir, "de manera mucho más eficiente en términos de calidad de vida".
El medicamento se ha registrado para Estados Unidos a través de un acuerdo de licencia alcanzado entre PharmaMar y Jazz Pharmaceuticals que está valorado en más de mil millones de dólares, de los cuales la biotecnológica española ha cobrado ya unos 300 millones por la firma del acuerdo y la aprobación de la FDA, y aún recibirá "cobros adicionales derivados de otros hitos que se van a producir en el futuro, además de importantes royalties por la venta del producto en Estados Unidos".
Mora recuerda que el norteamericano representa más del 55% del mercado mundial de productos de oncologÃa. A raÃz de esta aprobación, PharmaMar está hablando con potenciales socios en otras partes del mundo, donde ya tiene acuerdos para el sudeste asiático, Australia y China. "En Europa, el proceso regulatorio es diferente, aunque estamos en contacto con las autoridades para ver cuál es la mejor vÃa de registro aquÃ. No obstante, hemos abierto programas de uso compasivo o de medicación extranjera, para que también los pacientes en Europa puedan tener ya acceso al medicamento. En el primer semestre de este año -añade Mora-, ya hemos tratado a más de 600 pacientes en España, Francia y Holanda gracias al programa abierto de uso compasivo", lo que supone en su opinión "un dato increÃble que da idea de la gran necesidad que hay y de que es un producto que están aceptando muy bien los oncólogos".
La FDA designa medicamento huérfano a lurbinectedina para cáncer de pulmón microcÃtico
"Aplidin es el antiviral más potente que se ha descrito jamás"
'Yondelis' (PharmaMar) llegará por primera vez a Australia y Nueva Zelanda
De momento, la aprobación de la FDA convierte a Zepzelca en "el primer fármaco en llegar al mercado desde hace 24 años para la segunda lÃnea" de tratamiento del citado cáncer. "Esto nos pone en una posición de ventaja frente a competidores futuros, aunque no se prevén para los próximos tres años al menos en esta segunda lÃnea de tratamiento, por lo que, desde el punto de vista comercial, hay un espacio muy grande para el crecimiento del producto. Además, en oncologÃa llegar el primero es importante porque ya eres referente y te conviertes en tratamiento estándar, es decir, los productos posteriores que opten a la aprobación para la misma indicación tendrán que compararse con el primero, y superarlo tanto en actividad como en seguridad".
En cierto modo, PharmaMar ya ha experimentado esto con Yondelis para sarcoma en Europa, indicación con la que sigue manteniendo la misma cuota de mercado -del 30 al 35% en segunda lÃnea- desde su aprobación. "Después, otros productos se han aprobado para ese sarcoma, pero Yondelis mantiene la cuota inicial, es decir, se ha posicionado ya como un tratamiento de referencia para esa patologÃa".
El directivo recuerda cómo Yondelis marcó un hito en su dÃa porque fue la prueba de concepto de que el mar es una fuente de fármacos, y de que PharmaMar es capaz de desarrollarlos. Ahora, lurbinectedina marca su propio hito a otro nivel. "En Europa hay aproximadamente 12.000 diagnósticos anuales de sarcoma -para el está indicadoYondelis-, frente a los 65.000 de cáncer de pulmón microcÃtico que se diagnostican anualmente".
Comportamiento en el mercado
PharmaMar estima que pasados los primeros seis meses desde su introducción en el mercado americano podrá disponer de información suficiente para valorar la aceptación del compuesto y su comportamiento en el mercado ya en condiciones de uso real. "De aquà a final de año tendremos datos, aunque hay que ver cómo se comporta el mercado en la circunstancia actual provocada por la pandemia de Covid-19. En condiciones normales, entre 6 y 9 meses son suficientes para observar una tendencia fidedigna, aunque en Estados Unidos el posicionamiento definitivo se alcanza al tercer año", comenta Mora.
Pero el potencial de lurbinectedina se verá también con esas otras indicaciones para las que se está desarrollando, "en las que hay una necesidad médica importante –como mesotelioma y cáncer de endometrio- y para las que ha demostrado en estadios primarios de desarrollo una actividad interesante". PharmaMar está desarrollando esas otras indicaciones también con su socio Jazz, y ambas están trabajando en combinaciones de lurbinectedina con algunos productos de inmunoterapia, "demostrando con los primeros datos que están llegando una sinergia muy importante".
Su llegada al mercado constituye, por otra parte, "un espaldarazo muy importante para potenciar la investigación de la compañÃa, ya que en lo que queda de este año y en 2021 nuevos productos procedentes de nuestra investigación interna empezarán las fases clÃnicas", comenta el portavoz de PharmaMar, que también está trabajando para incorporar un nuevo producto de investigación externa a su red de ventas en Europa. Sin este espaldarazo esos nuevos productos entrarÃan en la clÃnica de uno en uno, mientras que la situación actual hace que este año sean tres los que van a empezar este proceso". En la actualidad, la biotecnológica tiene una cartera con más de 1.500 patentes fruto de su investigación, y filiales comerciales en varios paÃses de Europa.
Impacto económico
En definitiva, toda esta estrategia ha permitido a la compañÃa pagar dividendos recientemente -algo que Mora no recuerda que haya pasado con anterioridad después de 20 años en PharmaMar-, "y nuestro objetivo es tener una continuidad como negocio sostenible a futuro con incrementos de Ebitda que permitan esta nueva era", comenta e insiste, por último, en la definición de lurbinectedina como "un producto que nos transforma de ser una compañÃa con un solo compuesto en el mercado que comercializa directamente, a ser una compañÃa con indicaciones más grandes y con tres productos en el mercado en los próximos dos años, y que además se alimentará de importantes pagos de los socios por royalties, hitos, etc. Es decir, en dos años PharmaMar será otra empresa, fruto en gran medida de su apuesta por la investigación -más de 70 millones al año para poder llevar a cabo ensayos clÃnicos- hace algunos años cuando estaba en pérdidas".
En este sentido, Mora concluye que "se ha demostrado que los paÃses que han apostado por la investigación tienen una posición mucho más resistente y economÃas más saludables que la nuestra; originan patentes, acuerdos, traen dinero de fuera al paÃs y generan externalidades muy positivas y empleo de calidad", y pone el ejemplo de PharmaMar cuya plantilla está formada en un 85% por titulados universitarios, de los cuales el 22% son doctores en distintas materias.
- kuky24
- Mensajes: 501
- Registrado: 25 Feb 2019 15:32
- Agradecido: 58 veces
- Agradecimiento recibido: 41 veces
30/07/2020 13:42:31
PharmaMar rebota tras dejar atrás las pérdidas y ganar 114 millones hasta junio
PharmaMar rebota un 7% tras ganar 114 millones de euros hasta junio y dejar atrás los 21 millones de pérdidas registrados en el mismo periodo del año anterior.
Asà lo ha anunciado la farmacéutica a través de un hecho relevante remitido a la CNMV, en el que además subraya que ha cuadruplicado sus ingresos. PharmaMar sigue con sus cuentas afirmando que sus ventas han crecido un 35% en el periodo hasta situarse en los 52,5 millones de euros.
El principal impulso a este nivel de facturación proviene de los acuerdos de licencia y desarrollo, partida que arroja 115 millones, en contraste con los 630.000 euros del primer semestre de 2019, gracias al acuerdo alcanzado en Estados Unidos para la distribución de la lurbinectedina.
El resultado bruto de explotación (Ebitda), por su parte, fue de 119 millones de euros, frente al resultado negativo del año pasado, del que se desprende un margen del 92,7% sobre las ventas, a 30 de junio de 2020.
CORONAVIRUS
PharmaMar desarrolló en el mes de marzo sus propios kits de diagnóstico de Covid-19 y suscribió un acuerdo de distribución de test de técnica rápida de detección de anticuerpos para el virus, lo que ha supuesto unas ventas de 5,6 millones de euros, un 110% de incremento sobre el mismo periodo del ejercicio anterior.
En cuanto al segmento de oncologÃa, inició un ensayo clÃnico con Aplidina para el tratamiento de pacientes con Covid-19, cuyo objetivo es evaluar la eficacia y la seguridad de plitidepsin en los afectados que precisen ingreso hospitalario, actualmente en fase de reclutamiento de pacientes.
Pese a la llegada de la pandemia a España, el grupo no tuvo la necesidad de acogerse a medidas de regulación de empleo o de reducción de personal, ya que la actividad comercial no se vio afectada por la situación
PharmaMar rebota tras dejar atrás las pérdidas y ganar 114 millones hasta junio
PharmaMar rebota un 7% tras ganar 114 millones de euros hasta junio y dejar atrás los 21 millones de pérdidas registrados en el mismo periodo del año anterior.
Asà lo ha anunciado la farmacéutica a través de un hecho relevante remitido a la CNMV, en el que además subraya que ha cuadruplicado sus ingresos. PharmaMar sigue con sus cuentas afirmando que sus ventas han crecido un 35% en el periodo hasta situarse en los 52,5 millones de euros.
El principal impulso a este nivel de facturación proviene de los acuerdos de licencia y desarrollo, partida que arroja 115 millones, en contraste con los 630.000 euros del primer semestre de 2019, gracias al acuerdo alcanzado en Estados Unidos para la distribución de la lurbinectedina.
El resultado bruto de explotación (Ebitda), por su parte, fue de 119 millones de euros, frente al resultado negativo del año pasado, del que se desprende un margen del 92,7% sobre las ventas, a 30 de junio de 2020.
CORONAVIRUS
PharmaMar desarrolló en el mes de marzo sus propios kits de diagnóstico de Covid-19 y suscribió un acuerdo de distribución de test de técnica rápida de detección de anticuerpos para el virus, lo que ha supuesto unas ventas de 5,6 millones de euros, un 110% de incremento sobre el mismo periodo del ejercicio anterior.
En cuanto al segmento de oncologÃa, inició un ensayo clÃnico con Aplidina para el tratamiento de pacientes con Covid-19, cuyo objetivo es evaluar la eficacia y la seguridad de plitidepsin en los afectados que precisen ingreso hospitalario, actualmente en fase de reclutamiento de pacientes.
Pese a la llegada de la pandemia a España, el grupo no tuvo la necesidad de acogerse a medidas de regulación de empleo o de reducción de personal, ya que la actividad comercial no se vio afectada por la situación